KI-basierte Interpretation der ANA-HEp-2-IFA: Klinische Validierung in der Routinediagnostik
Der Nachweis antinukleärer Antikörper (ANA) mittels indirekter Immunfluoreszenz (IFA) auf HEp-2-Zellen gilt weiterhin als Goldstandard-Screeningverfahren für systemische autoimmune rheumatische Erkrankungen (SARD), einschließlich systemischem Lupus erythematodes, systemischer Sklerose und Sjögren-Syndrom1. Die manuelle Interpretation von ANA-HEp-2-IFA-Mustern ist jedoch zeitaufwendig, untersucherabhängig und unterliegt einer erheblichen Inter-Observer-Variabilität2.

Dieses Bild zeigt ein Laborgerät, den akiron® NEO, auf einer sauberen Arbeitsfläche. Eine Person mit weißem Laborkittel und blauen Handschuhen bedient das Touchscreen-Display mit dem Zeigefinger. Im Hintergrund ist ein Pipettenständer zu sehen, der die Laborumgebung bestätigt. Auf dem Bildschirm wird eine Datentabelle angezeigt, was darauf hinweist, dass das Gerät für Analyse- oder Testzwecke eingesetzt wird.
Eine kürzlich in Clinica Chimica Acta veröffentlichte groß angelegte Studie untersuchte, ob eine KI-basierte ANA-HEp-2-IFA-Interpretation unter realen Laborbedingungen die Leistung erfahrener Immunologinnen und Immunologen erreichen kann3. In die Untersuchung wurden 2.671 konsekutive Serumproben einbezogen, die in einem Routinediagnostiklabor analysiert wurden. Dabei wurde die visuelle Expertenauswertung mit der automatisierten Bildinterpretation mittels akiron® NEO verglichen. Die Analyse baut auf den soliden Ergebnissen einer vorangegangenen Pilotstudie auf, die bereits das Potenzial künstlicher Intelligenz zur Unterstützung der ANA-Diagnostik aufgezeigt hatte4.
Leistungsfähigkeit der automatisierten ANA-Diagnostik unter Realbedingungen
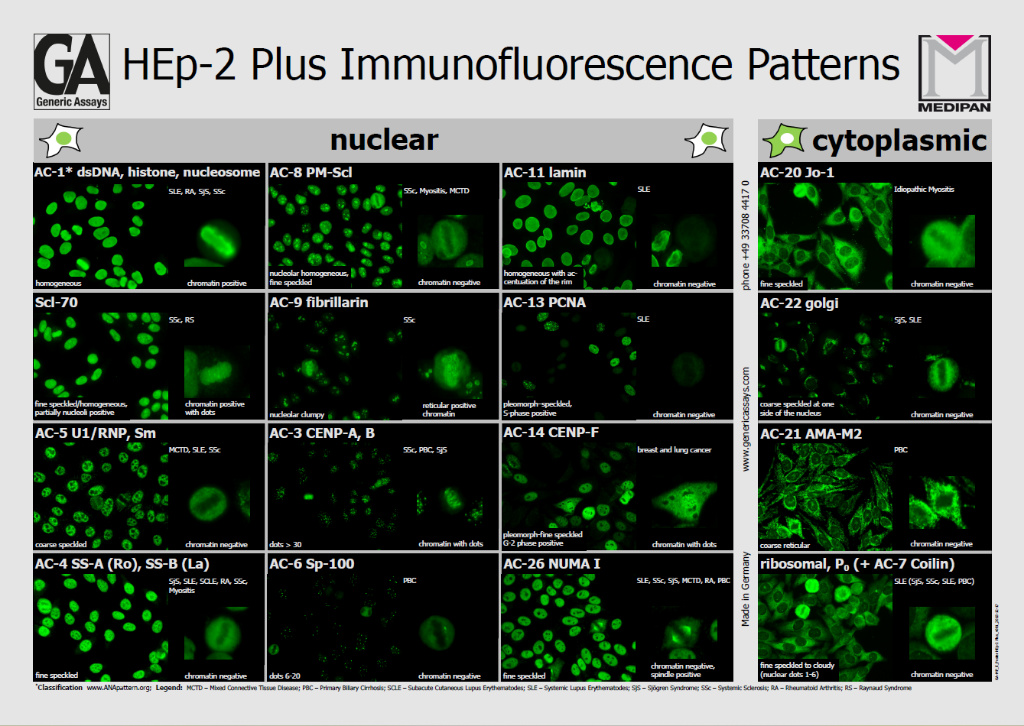
Bewertet wurden die Unterscheidung zwischen ANA-positiv und -negativ, die Titerzuordnung sowie die Erkennung von Fluoreszenzmustern gemäß dem International Consensus on ANA Patterns (ICAP) auf kompetentem Niveau.
Für die Klassifikation positiv/negativ zeigte sich eine gute Übereinstimmung (κ 0,616–0,699). Die Übereinstimmung verbesserte sich weiter, wenn schwach positive Proben ausgeschlossen wurden.
Auch die Mustererkennung erwies sich als robust. Nukleäre Muster erreichten bei klinisch relevanten Titern (≥1:320) Kappa-Werte von bis zu 0,650, während die Identifikation mitotischer Muster sogar noch höhere Übereinstimmungen erzielte (bis κ = 0,736). Zytoplasmatische Muster zeigten eine etwas geringere Konkordanz, was mit der in der Literatur beschriebenen inhärenten Variabilität in der ANA-Diagnostik übereinstimmt5.
Die Ergebnisse zeigen, dass die Übereinstimmung zwischen KI-gestützter Analyse und menschlichen Beobachtenden im gleichen Bereich lag wie die Inter-Observer-Übereinstimmung zwischen erfahrenen Immunologinnen und Immunologen. Dies bestätigt eine vergleichbare diagnostische Leistungsfähigkeit. Die Variabilität in der ANA-Interpretation spiegelt demnach eher die methodische Komplexität wider als eine technologische Limitation.
Das automatisierte System wies im Vergleich zu einer der menschlichen Bewertungen eine leicht geringere Gesamt-Positivitätsrate auf, was auf ein konservativeres Vorgehen bei Grenzfällen hindeutet. In Routinelaboren, insbesondere außerhalb spezialisierter rheumatologischer Zentren, kann eine solche Standardisierung dazu beitragen, unnötige Folgeuntersuchungen aufgrund unspezifischer schwach positiver Ergebnisse zu reduzieren.
Deep-Learning-Architektur zur ANA-Mustererkennung
Die akiron® NEO Plattform nutzt hierarchische Convolutional Neural Networks (CNNs), die für spezifische analytische Aufgaben trainiert wurden, darunter die Erkennung von Zellzyklusphasen, nukleären und zytoplasmatischen Mustern sowie die Analyse mitotischer Strukturen. Eine DAPI-Gegenfärbung unterstützt die präzise Identifikation der Metaphase, die für eine ICAP-konforme Klassifikation essenziell ist. Das System integriert diese Einzelanalysen zu einer standardisierten ANA-HEp-2-IFA-Befundung entsprechend der ICAP-Nomenklature.
Klinische Korrelation
In einer Subgruppe von Proben mit Reflex-Immunoblot-Testung zeigte die KI-basierte Mustererkennung erwartungsgemäße serologische Assoziationen. So korrelierten beispielsweise alle AC-3-Zentromer-Muster mit einer Anti-CENP-B-Positivität, während gesprenkelte Muster mit Anti-Ro52-, SS-A-, SS-B-, Sm- und U1-nRNP-Antikörpern assoziiert waren. Diese Ergebnisse stützen die klinische Validität der KI-gestützten ANA-Klassifikation.
Fazit
Die KI-basierte Interpretation der ANA-HEp-2-IFA zeigt in groß angelegten Routineanwendungen eine diagnostische Leistungsfähigkeit auf dem Niveau erfahrener Immunologinnen und Immunologen. Die fachärztliche Beurteilung bleibt weiterhin essenziell. Gleichzeitig verbessert die automatisierte ANA-Diagnostik die Workflow-Effizienz. Sie erhöht die Reproduzierbarkeit und reduziert die Subjektivität in der ICAP-basierten Musterklassifikation.
Für Labore, die eine standardisierte, skalierbare und hochdurchsatzfähige ANA-Testung anstreben, stellt die KI-gestützte HEp-2-IFA-Analyse mit akiron® NEO eine klinisch validierte und zukunftsfähige Lösung für die standardisierte ANA-HEp-2-Diagnostik dar.
Im Rahmen der Studie eingesetzte Produkte
| 4450 – akiron® NEO | IFA-Analysator mit KI-basierter Software zur automatischen Mustererkennung und Intensitäts-/Titerbestimmung von ANA, ANCA, nDNA und CytoBead®Technologie |
| 4063, 4065 – AKLIDES® ANA plus | HEp-2 cells based IFA for the determination of IgG antibodies against nuclear and cytoplasmic antigens (ANA) |
Entdecken Sie das vollständige Portfolio unserer IFA-Produkte
Literatur
- Bossuyt et al., (2020) Understanding and interpreting antinuclear antibody tests in systemic rheumatic diseases ↩︎
- Rigon et al., (2017) The inter-observer reading variability in anti-nuclear antibodies indirect (ANA) immunofluorescence test: a multicenter evaluation and a review of the literature ↩︎
- Schmidt et al., (2025) Comparison of manual with AI-aided interpretation of ANA HEp-2 IIF assay patterns in a clinical diagnostics lab ↩︎
- Mayr et al., (2025) Pilot Study of AI-Assisted ANA Immunofluorescence Reading—Comparison with Classical Visual Interpretation ↩︎
- Rigon et al., (2017) The inter-observer reading variability in anti-nuclear antibodies indirect (ANA) immunofluorescence test: a multicenter evaluation and a review of the literature ↩︎